文献背景
心力衰竭(HF)是心血管疾病的终末阶段,其在全球范围内造成了大量的致残率和死亡率。尽管采取了多种治疗策略,包括药物治疗、左心室辅助装置、人工心脏以及心脏移植等,心肌梗死(MI)后心力衰竭的进展仍具有极强的不可逆性。心脏修复是一种对缺血性心肌细胞坏死的保护性反应,包括左心室重构、血管重建和伤口愈合等。因此,对修复过程的治疗性调节或许有望预防心力衰竭并改善患者的预后。心脏补片,包括载有细胞的型补片和无细胞的型补片,已被证实能够改善心脏修复过程中的不良左心室重构。尽管载有细胞的补片取得了进展,但细胞种子的低保留率和植入率一直是一个主要问题。相比之下,无细胞补片易于定制、实用且在临床转化方面前景广阔。迄今为止,关于无细胞心脏补片的研究分别侧重于优化机械性能以抑制梗死心肌,或优化微结构,例如孔隙、微通道或纳米纤维,以促进血管再生。然而,同时具备仿生机械性能和促血管生成特性的多功能心脏补片的制造仍然具有挑战性。此外,局部药物输送作为一种有益的策略,用于增强疗效并以低剂量减少全身毒性副作用,也受到了关注。已报道的水凝胶、纳米颗粒和载药支架可以维持治疗试剂的释放,以促进心脏修复。然而,这些构建体的疗效和稳定性仍需提高。
为了克服上述障碍,上海交通大学医学院附属瑞金医院的叶晓峰、赵强团队,联合东华大学材料科学与工程学院的游正伟团队设计了一种可渗透、多功能的心外膜装置,称为PerMed,它是通过生物弹性体(BEP)、微血管化材料(PHMs)和输送系统组装而成的。PerMed建立了一个协同的机械和生物环境,能够有效降低壁应力和心肌细胞凋亡,改善左心室应变,并促进血管重建和心脏代谢。由于其良好的机械性能和弹性,PerMed具有适合微创手术植入的结构,该研究团队还为PerMed设计了一种匹配的爪形固定器,使其能够在大型动物(猪)模型的心外膜表面轻松且牢固地固定,其在临床应用中具有治疗心脏病的潜力。

题目:A perfusable, multifunctional epicardial device improves cardiac function and tissue repair
期刊:Nature medicine
影响因子:50
PMID:33723455
DOI:10.1038/s41591-021-01279-9
通讯作者:叶晓峰,游正伟,赵强
作者单位:上海交通大学医学院,东华大学
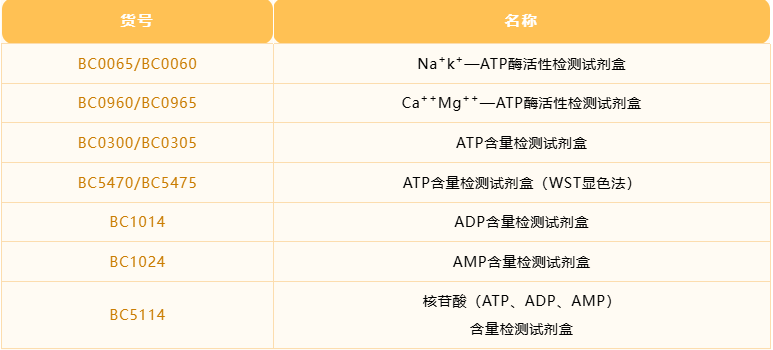
索莱宝合作产品:
产品名称:
ATP含量检测试剂盒
产品货号:
BC0304
摘要
尽管在心肌梗死(MI)后的心脏修复技术方面取得了进展,但仍需要开发新的综合治疗方法。这项研究设计了一种可灌注、多功能的心外膜装置(PerMed),该装置由一种可生物降解的弹性贴片(BEP)、可渗透的分级微通道网络(PHMs)以及一个能够通过皮下植入泵输送治疗剂的系统组成。其具有弹性良好、促血管再生、改善局部微循环、精准持续药物递送、生物可降解性以及生物相容性良好的特点。在植入心外膜后,BEP用于为心室重塑提供机械刺激,而PHMs用于促进血管生成并允许修复细胞的浸润。在心肌梗死的大鼠模型中,PerMed的植入改善了心室功能。当与泵连接时,PerMed能够实现血小板衍生生长因子-BB的定向、持续和稳定释放,与没有泵的装置相比,增强了心脏修复的效果。此外该团队还证明了在猪身上进行微创手术植入PerMed的可行性,展示了其在临床转化治疗心脏病方面的潜力。
研究内容及结果
1装置设计与材料表征
PerMed是一种创新的多功能心外膜设备,由三大核心组件构成:生物可降解弹性贴片(BEP)、渗透性分层微通道网络(PHMs)和药物输送系统(图1a-b)。该设备通过协同作用实现心肌修复的多重功效。
在材料特性方面,PGS/PCL(9:1)BEP表面均匀光滑(图1c),而PCL比例增加(如8:2、7:3)会导致相分离;PCL/明胶(3:1)PHMs具有多层互联分支网络,通道壁分布均匀微孔(5μm)(图1d),而明胶比例增加(1:1)会导致结构塌陷。在机械性能方面,PGS/PCL(9:1)BEP拉伸模量(1.61±0.26MPa)介于纯PGS(0.8MPa)和PCL(12MPa)之间,匹配心肌组织力学需求,在40%应变下循环拉伸/压缩10次后,滞后率<10%,表明优异弹性恢复能力(图1f-g);PCL/明胶(3:1)PHMs压缩模量(12.75±1.73kPa)适合动态心脏变形(图1h),40%应变循环压缩后结构无塌陷,维持管状通道(图1i)。在生物降解性与生物相容性方面,PGS/PCL(9:1)在皮下84天降解77.3%,降解速率介于快速降解的PGS(>90%)与缓慢降解的PCL(<20%)之间,其表面心肌细胞(NRCMs)和ADSCs黏附良好,细胞活性与纯PGS或PCL无差异;PCL/明胶(3:1)在体内28天保持结构完整,微孔率无显著下降,支持心脏成纤维细胞(CFs)和脂肪干细胞(ADSCs)高存活率(>90%),并形成3D细胞网络(图1j-k)。
PGS/PCL(9:1)的平衡力学性能(弹性模量≈心肌)与降解速率,成为理想机械支撑材料。PCL/明胶(3:1)以仿生微通道结构和优异亲水性,促进细胞浸润与血管再生。两者均支持细胞高活性,且未引发显著免疫排斥,满足长期植入需求。BEPs核心功能为力学支撑(抑制扩张、改善收缩),PHMs核心功能为血管再生与细胞浸润,但是,两者的独立作用均存在局限,需联合以实现全面修复。
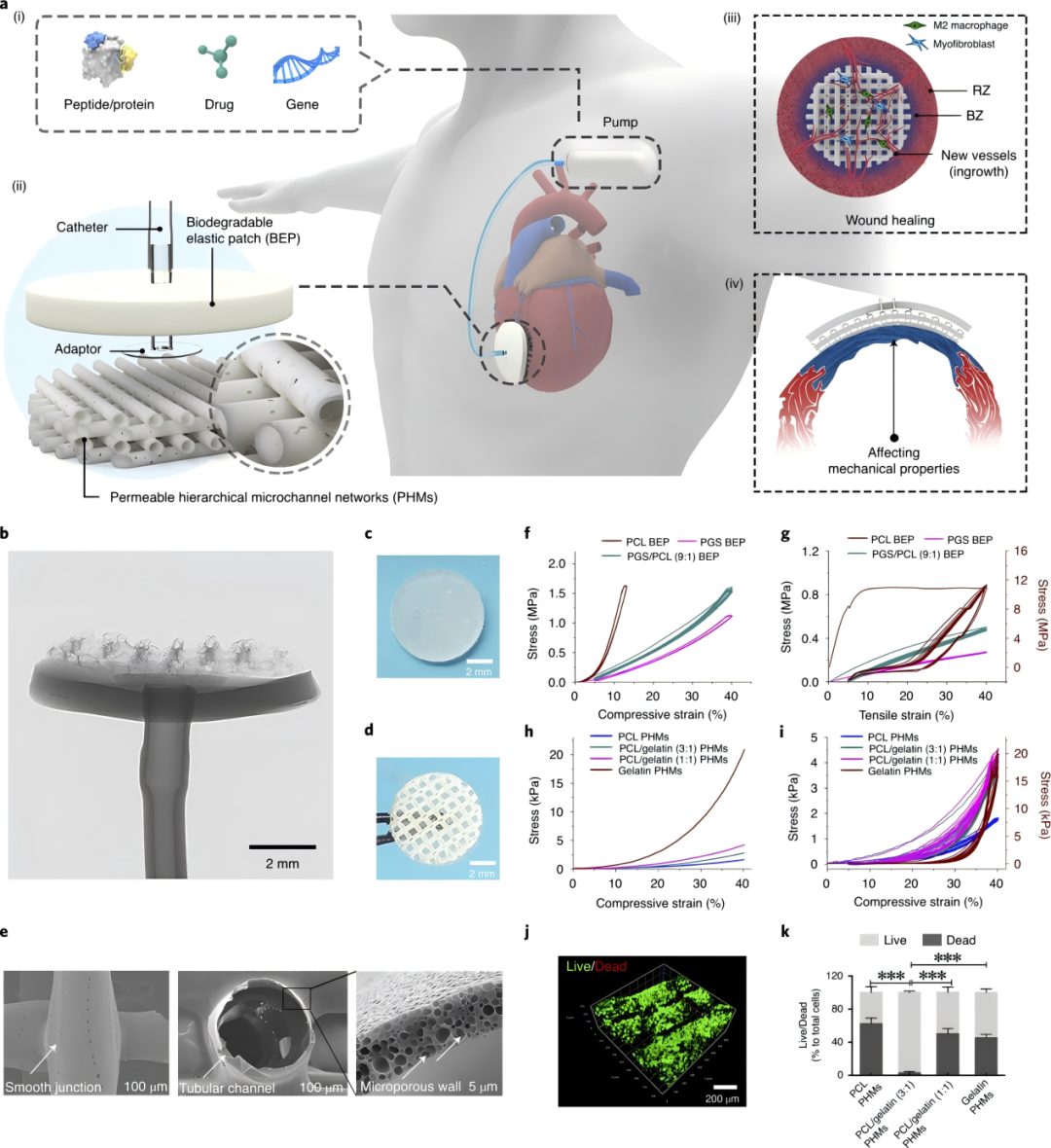
图1:PerMed设备的设计与表征。
2 心脏功能与结构的改善
PerMed装置改善了心功能恢复,限制了不良左室重构。大鼠心肌梗死(MI)模型分为5组:假手术组、MI组、PerMed(PCL)、PerMed(PGS)、PerMed(PGS/PCL)(图2a),评估28天内心功能(超声、cMRI、PET)和组织修复(Masson染色)。结果发现,PerMed(PGS/PCL)组生存率显著高于MI组(P<0.05)(图2b)。MI组的LVEF(左心室射血分数)和LVFS(左心室缩短分数)显著下降,而PerMed(PGS/PCL)组的LVEF和LVFS适度上升(图2c-d),心功能提高;心脏磁共振成像(cMRI)显示,PerMed(PGS/PCL)组的心室扩张(LVEDD、LVEDV)和纤维化面积显著减少,心肌壁厚度增加(图2e-g),重塑心室;PET显示PerMed(PGS/PCL)组的心肌存活率(SUV值)最高,梗死面积最小(图2h-i),心肌代谢提高。接下来评估了PerMed对左心室重构的影响。首先,正电子发射断层扫描(PET)结果显示,PerMed (PGS/PCL)组的总梗死面积小于其他组(图2j),其次,马松三色染色显示,PerMed (PGS/PCL)组的纤维化组织面积减少(图2k,l),左心室壁厚度增加(图2k-m);最后,PerMed (PGS/PCL)组位于边界带(BZ)和远隔区(RZ)的心肌细胞横截面积显著低于其他组(图2n-o)。因此,PerMed,尤其是PerMed (PGS/PCL),似乎能够改善心脏功能并限制不良的左心室重构。
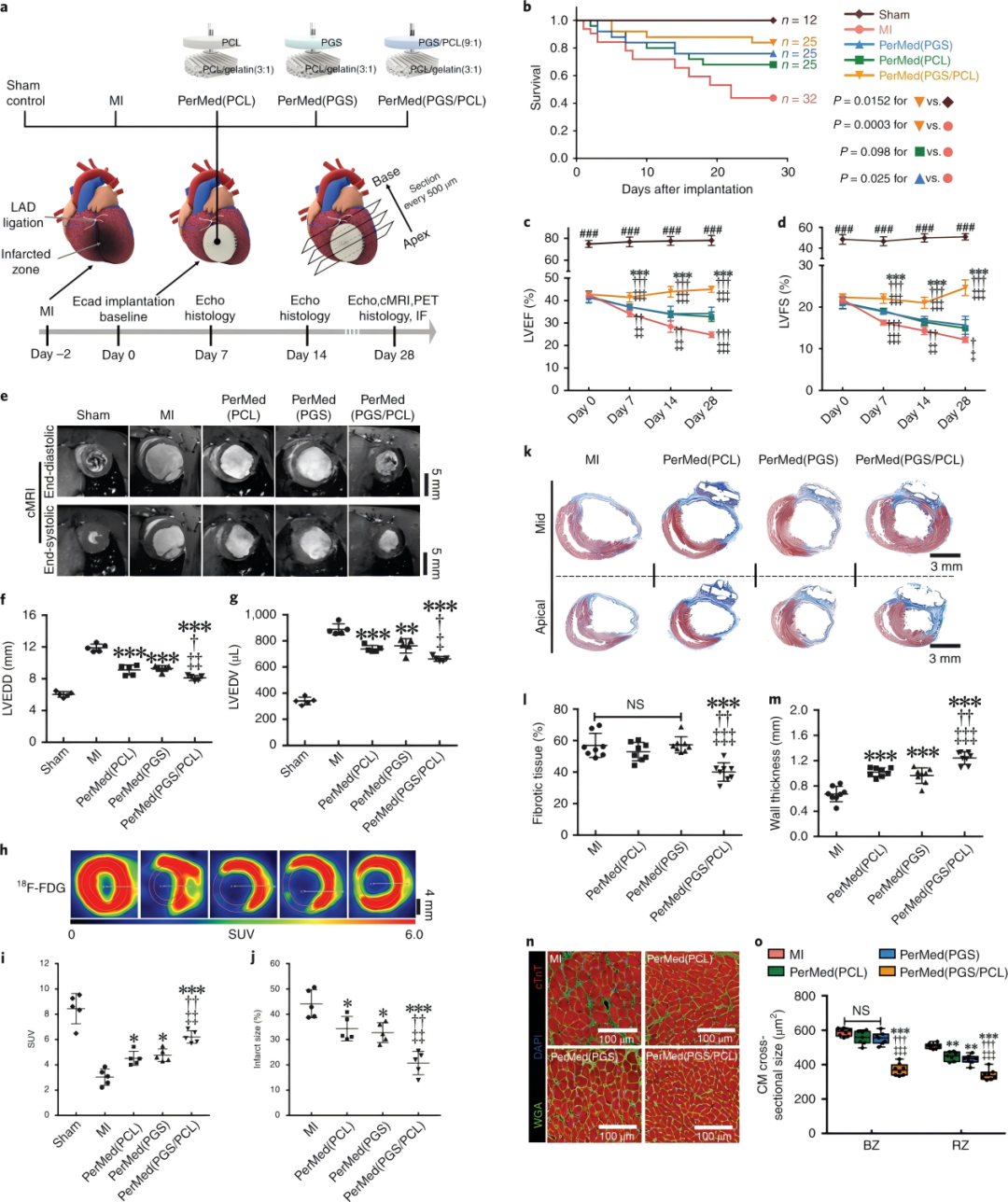
图2:PerMed装置改善了心肌梗死大鼠模型的心功能恢复,限制了不良左室重构。
3 力学机制与细胞外基质重塑
PerMed通过改善心肌力学性能和促进组织修复双重机制显著增强心脏功能。区域应变分析显示,PerMed (PGS/PCL)组在第28天表现出最佳的左心室径向应变(LVErr)和周向应变(LVEcc)恢复(图3a-d),对左心室收缩末期壁增厚(LVWT)的区域分析也得出了相似的结果(图3e)。同时使梗死区(IZ)和边缘区(BZ)的壁应力显著降低(图3f-g)。这种力学改善伴随着活跃的组织修复过程,免疫荧光显示肌成纤维细胞在PHMs通道和梗死区大量浸润(扩展数据图7a-c),同时M2型巨噬细胞在植入后第14-28天显著增加(扩展数据图8d-e),形成促再生微环境。更重要的是,PerMed (PGS/PCL)诱导了有利的胶原重塑,使胶原III/I比值在设备界面(图3i)、梗死区(图3j)和边缘区(扩展数据图9f)均显著提高。这些结果表明PerMed通过协同优化心肌力学环境和促进修复细胞介导的组织重塑,实现了对心肌梗死的多维度治疗。

图3:PerMed植入术后管壁应力、径向和周向应变及胶原亚型的区域评价。
4 血管生成与细胞保护效应
PerMed (PGS/PCL)展现出显著的促血管生成和代谢改善作用。通过isB4染色和CD31/α-SMA免疫荧光证实,该设备不仅促进毛细血管再生(图4a-b),还显著增加BZ区和PHMs内的动脉密度(扩展数据图10-11)。18F-FDGPET成像显示PerMed (PGS/PCL)组心肌细胞代谢活性显著提升(图4c-d),同时线粒体形态和功能明显改善,线粒体呈现规则棒状排列(扩展数据图12a)PerMed (PGS/PCL)组的线粒体密度和分割率(%)低于其他PerMed组(图4e和扩展数据图12c),ATP生成增加(图4f),线粒体生物发生相关基因(Ppargc1a、Pink1和Opa1)表达上调(扩展数据图13)。此外,TUNEL检测表明PerMed (PGS/PCL)能有效抑制BZ区心肌细胞凋亡(图4g)。这些结果证实PerMed (PGS/PCL)通过协同促进血管新生、改善能量代谢和抑制细胞凋亡等多重机制,全面改善了梗死心肌的微环境。
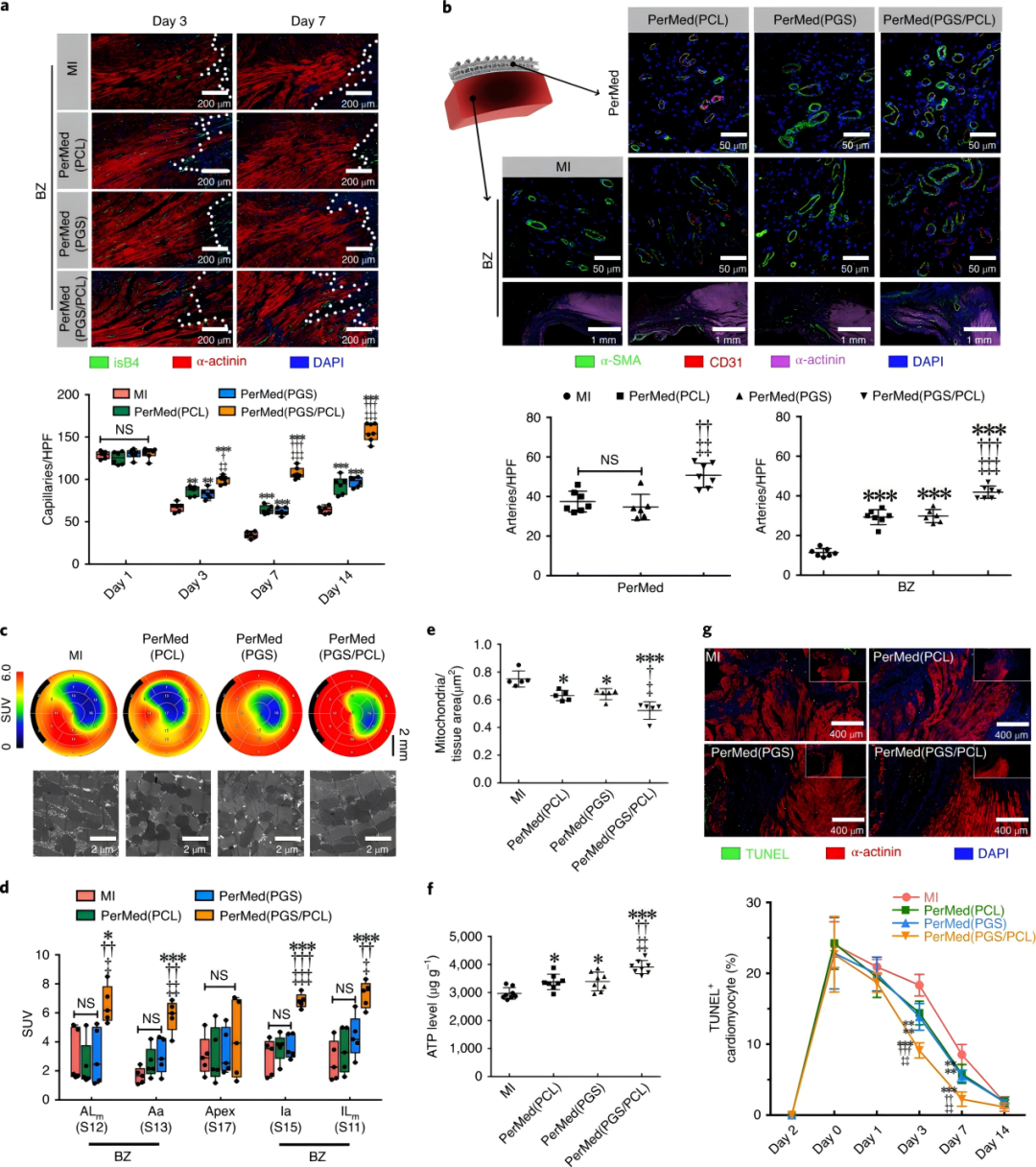
图4:PerMed (PGS/PCL)装置改善血管生成和心脏代谢,减少心肌细胞凋亡。
5 药物控释系统性能
PerMed展现出卓越的物质递送性能。其微通道网络(PHMs)可实现治疗剂的均匀灌注,体外实验证实亚甲蓝和造影剂能有效扩散(图5b,扩展数据图14a)。微CT显示植入后28天内PHMs孔隙率保持稳定(扩展数据图7c),且纤维化未显著影响物质扩散,AAV9-GFP在心肌细胞和肌成纤维细胞中成功表达(扩展数据图8),18F-FDGPET-CT证实小分子药物可有效从PerMed向心肌组织转运(图5c-d)。更重要的是,连接渗透泵的PerMed能维持Cy7-BSA持续释放28天(图5e-f),而手动灌注组4天内即失效。此外,设置了无泵组、PBS组和血小板衍生生长因子-BB(PDGF-BB)组三个组别,并从心脏功能和心脏代谢方面对它们进行了比较,检验PerMed通过持续释放血小板衍生生长因子-BB来增强心脏修复的效果(图5g)。功能验证表明,持续释放PDGF-BB显著增强治疗效果,cMRI显示PDGF-BB组LVEF提高(图5h),分析左心室舒张末期容积(LVEDV)和左心室收缩末期容积(LVESV)的结果相似(图5i)PET证实心肌代谢活性增强(图5j),组织学分析显示NG2+周细胞包裹的新生血管数量增加60%(图5k-m),血管成熟度显著改善。这些结果证明PerMed通过优化的物质扩散特性和可控释放系统,为心脏修复提供了高效的递送平台。
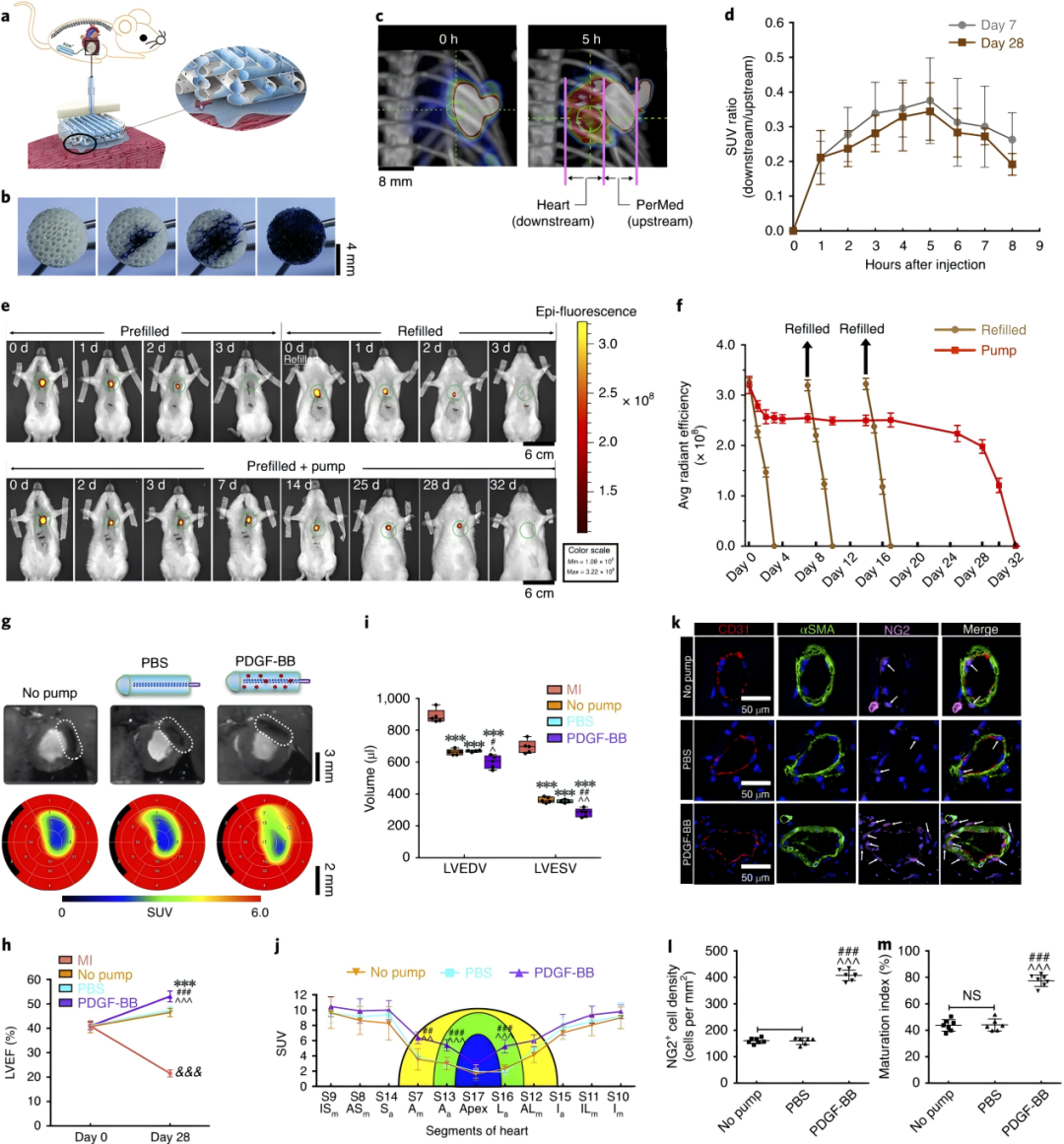
图5:PerMed用于治疗试剂缓释的靶向递送系统的性能。
6 大型动物植入可行性
PerMed在大型动物模型中展现了优异的临床转化潜力。通过设计的爪形固定器(由中心环和多臂钩针组成(图6a和扩展数据图10a-b),直径3cm、厚2mm的弹性PerMed装置可在胸腔镜引导下经微创切口植入(图6b-c),无需缝合即牢固锚定于左心表面(扩展数据图10c-f)。植入过程视频记录显示(补充影片6),装置能完美贴合跳动的心脏形态(扩展数据图10f),验证了其优异的组织适应性和手术可行性。验证了PerMed在大型动物中的可行性和微创植入潜力,为临床转化奠定基础。
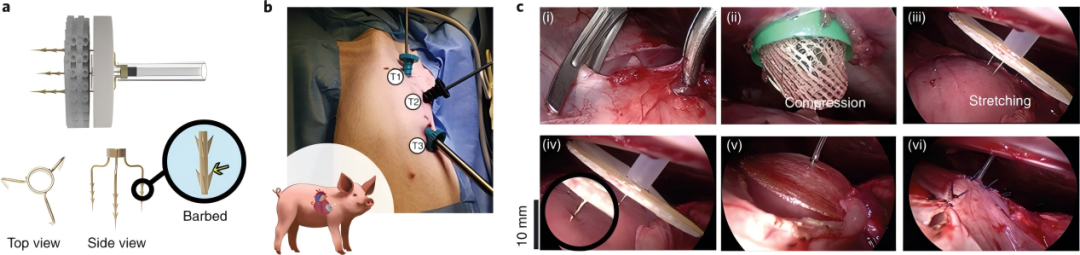
图6:一种先进PerMed装置在猪体内的微创手术植入。
结论
在这项研究中,团队聚焦于心肌修复领域的关键难题,成功研发出PerMed心外膜修复系统。该系统代表了当前心肌修复技术的重要突破,其创新性地整合了三大核心技术模块:首先,采用仿生设计的BEP弹性补片具有与天然心肌组织相匹配的力学性能,能够为受损心脏提供精准的力学支撑,有效抑制心室不良重构;其次,创新的PHMs微血管网络通过其独特的分层多孔结构设计,不仅显著促进血管新生,更为各类修复细胞构建了高效的迁移通道;最后,智能化的药物输送系统可实现多种治疗因子(包括药物、基因和生长因子等)的持续稳定释放。这一系统的独特优势在于:采用微创植入技术显著降低手术创伤,其专门设计的爪形固定器已在大型动物实验中证实了优异的稳定性和适配性;同时,装置84天的持续治疗效果验证了其长期有效性,而机械支撑与生物修复的双重协同机制更确保了全面的治疗效果。特别值得一提的是,PerMed系统展现出的良好生物相容性和可控降解特性,使其成为目前最具临床转化前景的心肌修复解决方案,该研究为心肌梗死后的综合治疗提供了新策略,也具有显著的临床转化潜力。
索莱宝产品亮点
 相关产品
相关产品