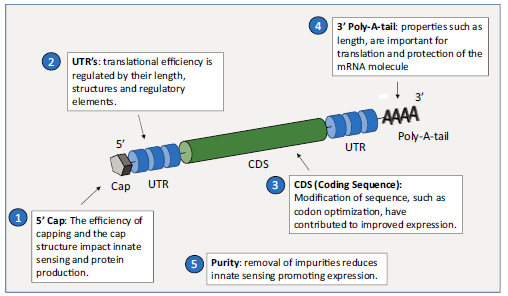
mRNA又称为信使RNA,是以细胞核中双链DNA的一条链作为模板转录而来,携带着DNA上的遗传信息,负责指导蛋白合成。mRNA疫苗的原理是将编码疾病特异性抗原的mRNA经改造后注射到人体中,利用宿主的细胞工厂合成抗原蛋白,从而训练免疫系统进行抗原识别、免疫应答并形成记忆,起到预防疾病的作用。
mRNA技术的发展历史仅有短短数十年(图2)。1961年,加州理工学院的科学家首次发现了mRNA这种介于DNA和蛋白表达中间的“信使”。1990年,一项实验发现注射到小鼠中的外源性mRNA可以表达出目标蛋白并产生免疫反应,首次揭示mRNA可作为疫苗的前景。1992年,又有研究表明编码加压素的mRNA注射到小鼠大脑,可以提高加压素的表达以缓解尿崩症,显示出mRNA具备成为治疗性药物的潜力。
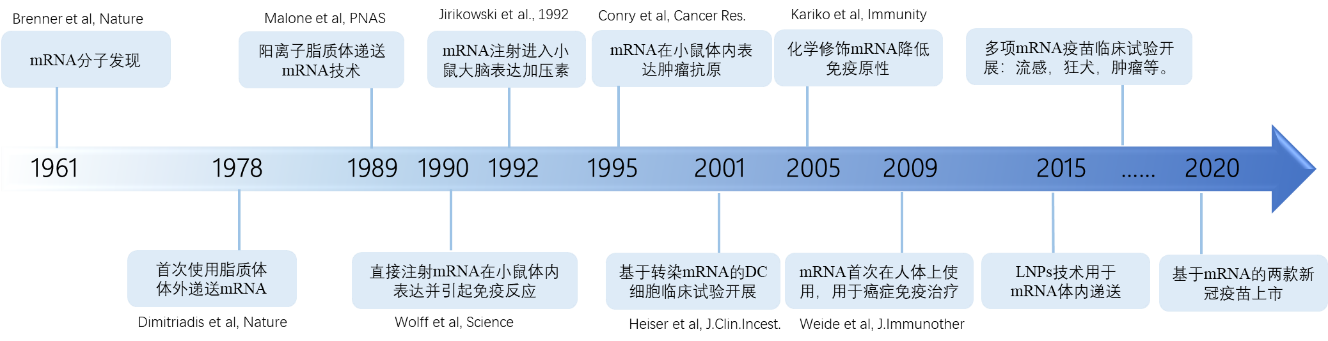
图2. mRNA技术发展历程
>>>>技术瓶颈
2. 由于环境中存在很多可以降解mRNA的酶,导致mRNA在递送过程中被降解,体内递送效率不高。
相比传统疫苗,mRNA疫苗技术具有三点突出优势,即快速、安全和高效。
1. mRNA疫苗最大的优势在于研发和生产周期短。面临快速传播的传染病危机,疫苗公司的最大挑战不再仅仅是有效性,而是如何能够在最短的时间内对疫情做出最快的反应,能够大规模、低成本地生产出社会需要的疫苗。mRNA疫苗只需要掌握病毒的基因序列,就可以在几周内设计和构建出成品疫苗。在新冠病毒基因序列公布仅42天后,Moderna就研发出第一批可用于临床试验的疫苗。进入生产阶段后,由于mRNA疫苗的生产不需要细胞培养、抗原提取等过程,工艺相对简单,疫苗能够迅速量产。此外,面对容易产生基因组突变的病毒,mRNA疫苗也能够灵活应变,只要改变mRNA序列,就可以在1-2个月内推出新一代疫苗,能够有效防止变种病毒逃逸人体的免疫识别。
2)mRNA疫苗无佐剂,从而减少由佐剂导致的不良反应发生;
3)mRNA疫苗的生产不需要动物源性的细胞,因此避免了可能存在的生物毒性;
4)mRNA疫苗不需要像灭活病毒疫苗那样大量培育活病毒,可以避免活病毒泄露的风险。
目前关于mRNA疫苗的安全问题还有一个令人关心的议题,即mRNA疫苗是否会改变人体细胞中的DNA遗传物质。实际上,mRNA在翻译出蛋白后会在细胞微环境中自然降解,仅在宿主细胞中短暂存在,因此mRNA不会进入细胞核与人体基因组相互作用,逆转录整合进入宿主基因组的风险和诱导宿主基因突变的风险都很低。当然,对于这种全新机制的疫苗,少不了在临床应用中持续进行安全性监测,以完善对疫苗安全性的验证。
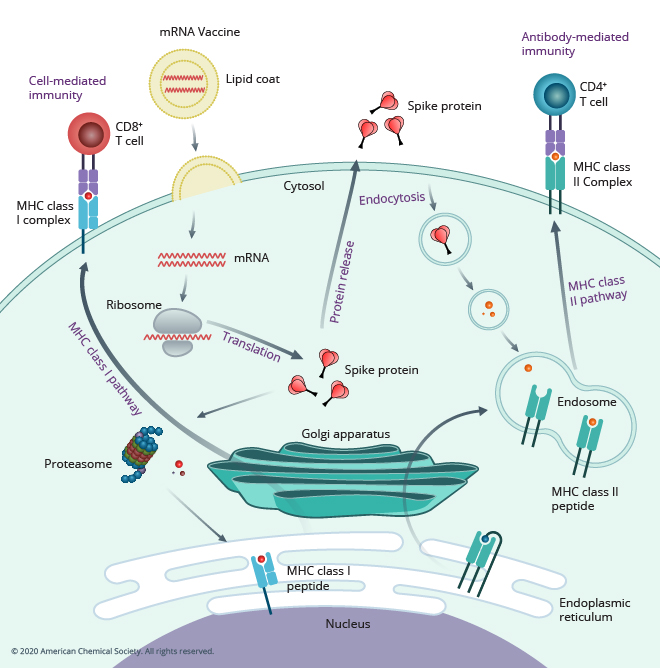
目前全球范围内大规模接种的两款mRNA疫苗分别是Pfizer-BioNTech的BNT1262b2和Moderna的mRNA-1273。在疫苗设计上,这两款疫苗都采用脂质纳米颗粒(LNPs)递送编码全长刺突蛋白(Spike)的mRNA,并在Spike蛋白基因序列上的K986和V987两个位点做了脯氨酸(proline)突变以使表达出来的S蛋白稳定在融合前(Pre-fusion)构象,更有利于免疫系统识别新冠病毒。在三期临床实验中,这两款疫苗分别被证明具有95%和94.5%的保护效力。目前,两家公司都在加速疫苗生产,Moderna原预计今年的疫苗产量将达到8亿-10亿剂,辉瑞计划到2021年底生产25亿剂新冠疫苗。
目前的两款mRNA疫苗都需要-70℃(BioNTech)或-20℃(Moderna)的冷链运输和保存才能保证mRNA的稳定性,这是发展中地区接种的一大受限因素。因此,mRNA疫苗一个重要的优化方向是设法降低苛刻的低温要求。目前,Moderna正在开发热稳定性更好的二代疫苗mRNA-1283,已接近一期临床试验阶段。苏州艾博开发的ARCoV疫苗经动物实验验证具有较好的热稳定性,在2-8℃环境下可以长期保存,在室温下可以存储至少一周。这款我国自主研发的疫苗预计在今年10月底完成临床试验的初步研究。
为了持续优化mRNA疫苗的有效性,科学家们需要经过更深入的研究全面地了解mRNA疫苗的作用机制。为了确保疫苗的长期有效性和安全性,mRNA新冠疫苗三期临床试验对象也需要持续追踪。mRNA技术未来还涉及许多值得探究的问题,包括如何通过基因编辑进一步提高mRNA的翻译效率和稳定性;能够进行自身复制(self-amplifying)的mRNA是否会更有利于增强免疫原性;为扩大疫苗接种率,如何设计出使用更便捷、侵入性更弱的鼻喷式mRNA疫苗;免疫水平下降后,是否有必要再次接种一剂甚至多剂mRNA疫苗;mRNA疫苗在特殊人群中的适用性,如高龄老人、儿童、孕妇、免疫系统缺陷病人等。
如今,mRNA疫苗的概念不仅局限于新冠病毒,还广泛应用于其它传染性疾病(人类呼吸道合胞病毒、狂犬病毒、寨卡病毒、艾滋病病毒等)、肿瘤免疫和遗传性疾病等领域的疫苗或药物开发(图4)。从新冠疫苗起步,到癌症治疗,未来mRNA技术或许能够攻克更多领域的难题,为人类带来新的希望。
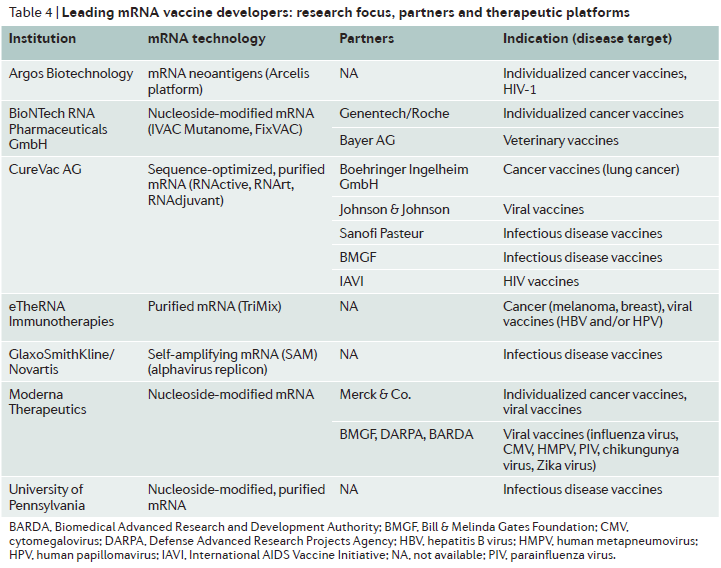
图4. mRNA疫苗主要研发公司和研究机构,其研究方向、合作伙伴及应用平台
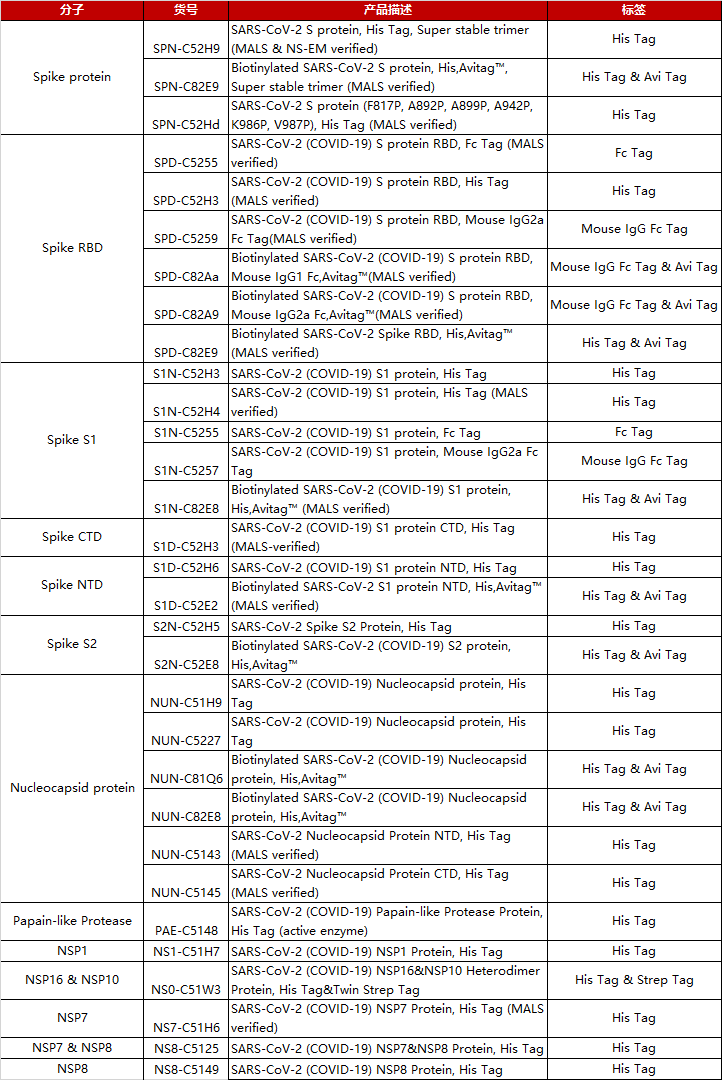
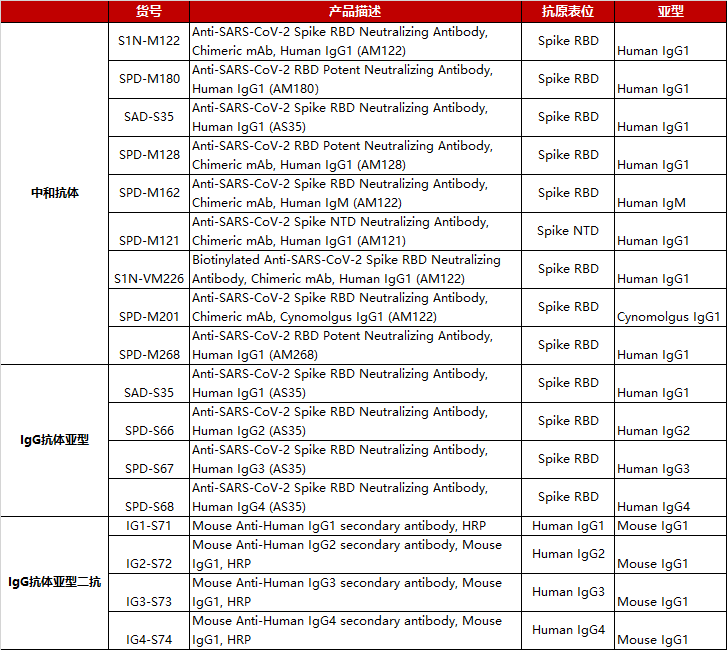
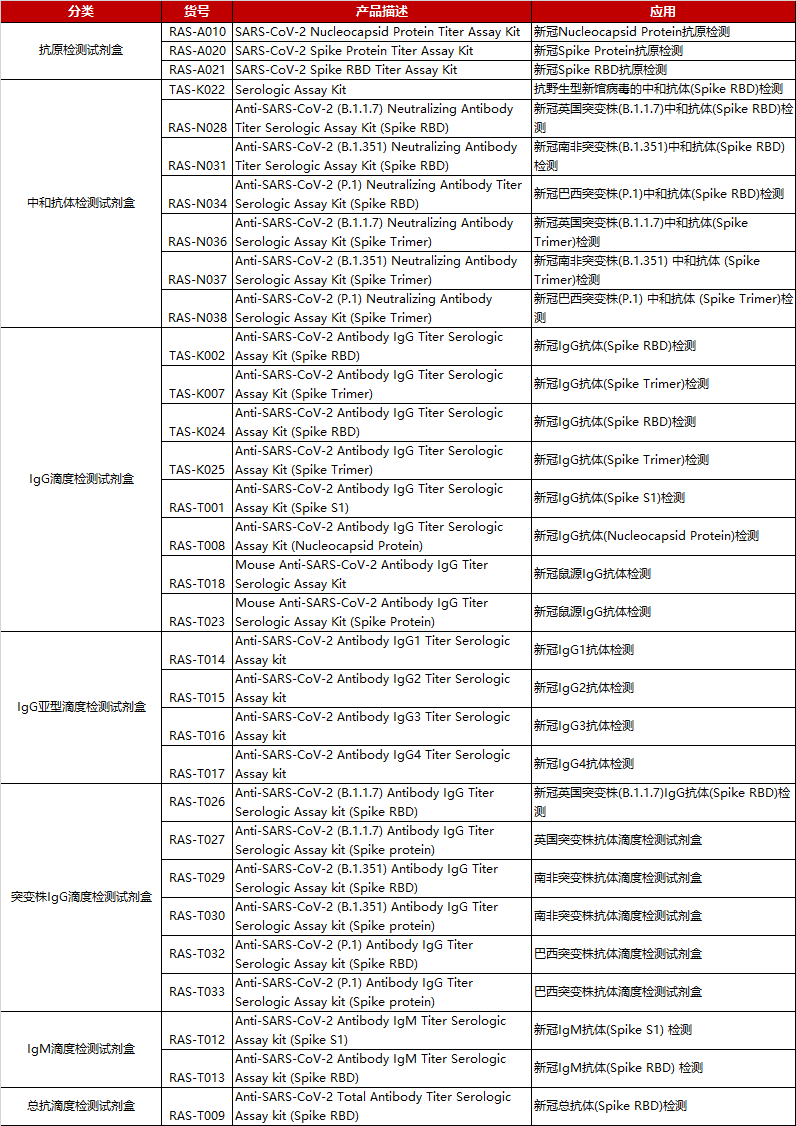
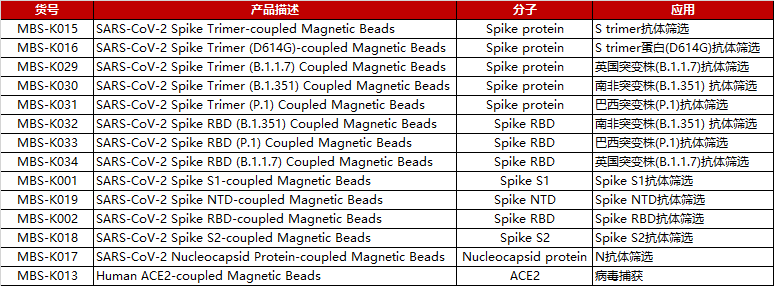
ACRO生产的蛋白产品具备高纯度、高稳定性、批间差小等优势,适用于Western blot/ELISA/SPR/BLI等各种实验,服务于准确、高效的疫苗相关研究。
新冠突变株抗原
点击下表中文字内容了解各突变株详细产品信息
|
种属 |
抗原表位 |
标签 |
|
Spike S1 Spike protein |
His Tag |
|
|
Spike RBD Spike S1 Spike NTD Spike S2 Spike protein Nucleocapsid protein |
His Tag |
|
|
Spike S1 Spike NTD Nucleocapsid protein |
His Tag |
|
|
|
His Tag |
|
|
|
His Tag |
|
|
|
His Tag |
|
|
|
His Tag |
|
|
Spike RBD |
His Tag |
|
|
Spike RBD |
His Tag |
|
|
|
His Tag |
|
|
Spike RBD |
His Tag |
> SARS-CoV-2 其它突变株 Othervariants
> SARS-CoV-2 高频N突变 Nucleocapsid protein mutations
马上扫码入群,了解疫苗领域热点信息吧~

(请备注:公司+姓名+疫苗)
现申请入群还可获取新冠疫苗峰会mRNA疫苗前沿进展解读精彩报包,快来申请吧~
相关阅读:
> 全球新冠疫苗研发峰会报告深度解读(内含福利)
> 都是mRNA疫苗,辉瑞和莫德纳的新冠疫苗有什么不一样?(内附FDA专家组答辩PPT)
> 重组蛋白疫苗:新冠疫苗中的“后浪“
参考文献:
1. Cross, R. Without these lipid shells, there would be no mRNA vaccines for COVID-19. March 6, 2021. Volume 99, Issue 8, Chemical & Engineering News. Retrieved from https://cen.acs.org/pharmaceuticals/drug-delivery/Without-lipid-shells-mRNA-vaccines/99/i8
2. First Participants Dosed in Phase 1 Study Evaluating mRNA-1283, Moderna’s Next Generation COVID-19 Vaccine. March 15, 2021. Retrieved from https://www.businesswire.com/news/home/20210315005475/en/
3. 英珠,李.攻克COVID-19的希望新秀—mRNA疫苗. September 2nd, 2020. CAS American Chemical Society. Retrieved from https://www.cas.org/zh-hans/resource/blog/covid-mrna-vaccine
4. Amanat F, Strohmeier S, Rathnasinghe R, et al. Introduction of two prolines and removal of the polybasic cleavage site leads to optimal efficacy of a recombinant spike based SARS-CoV-2 vaccine in the mouse model. bioRxiv [Preprint]. Sep 17, 2020. doi: 10.1101/2020.09.16.300970. Retrieved from https://pubmed.ncbi.nlm.nih.gov/32995785/
5. Jackson, N.A.C., Kester, K.E., Casimiro, D. et al. The promise of mRNA vaccines: a biotech and industrial perspective. npj Vaccines 5, 11 (2020). https://doi.org/10.1038/s41541-020-0159-8
6. Pardi N, Hogan MJ, Porter FW, Weissman D. mRNA vaccines - a new era in vaccinology. Nat Rev Drug Discov. 2018 Apr;17(4):261-279. doi: 10.1038/nrd.2017.243. Retrieved from https://pubmed.ncbi.nlm.nih.gov/29326426/

您可通过以下方式联系到ACROBiosystems:
邮件:inquiry@acrobiosystems.com
电话:15117918562
(备注:姓名+公司)