2021年3月,中国科学院微生物研究所与安徽智飞龙科马生物制药有限公司联合研发的重组蛋白新冠疫苗在国内和乌兹别克斯坦获得紧急使用批准,成为我国获批正式上市的第一款重组蛋白疫苗。该疫苗在已完成的I、II期和正在进行的III期临床试验中,均展现出很好的安全性和免疫原性。该疫苗使用了新冠刺突蛋白RBD二聚体作为亚单位抗原,原理是将编码RBD的基因片段串联起来,以重组表达同型二聚体(图1)。据报道,这种二聚化可以增加抗原的稳定性,在重组表达SARS-CoV和MERS-CoV抗原中也有应用先例。我国自主研制的疫苗为应对新冠疫情提出了一种成熟的解决方案,这无疑是一个好消息。
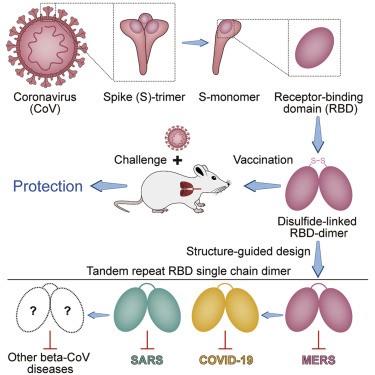
图1 一种通用的β冠状病毒疫苗设计1
作为预防和控制传染病最有效、最经济的手段,新冠疫苗的研发进展一直倍受关注。迄今为止,全球已有14种疫苗获得政府公共卫生部门正式批准使用,仍在开发中的疫苗有18种处于III期大规模实验阶段,44种处于II期扩展实验阶段,31种处于安全剂量测试的I期实验阶段。这些疫苗的开发应用了多种技术路线,除了最早问世的mRNA疫苗,我国普遍接种的灭活病毒疫苗,还包括了病毒载体疫苗、重组蛋白疫苗等(图2)。其中,重组蛋白疫苗,又称基因工程重组亚单位疫苗,在众多疫苗技术中正展现出良好的应用前景,受到了越来越多的关注。

图2 不同类型疫苗对比
新冠重组蛋白疫苗的的技术原理是表达生产出新冠病毒感染人体细胞的关键“部件”——刺突蛋白,将其注射到人体后可刺激免疫系统产生阻止新冠病毒感染人体细胞的中和性抗体。在过去的几十年中,重组蛋白技术已经成为安全高效、相对便宜,在微生物和其它宿主表达系统中均可广泛使用的技术。目前,全球已有2款重组蛋白疫苗被批准使用,8种已进入三期临床试验,处于二期和一期临床阶段的重组蛋白疫苗在所有疫苗种也占有相当高的比例(图3)。
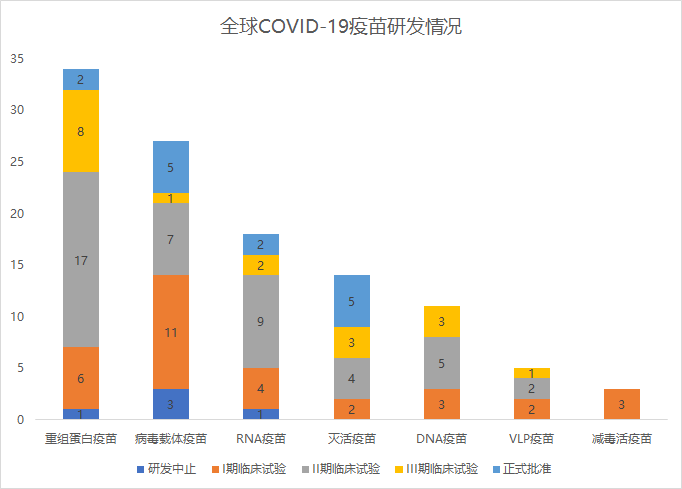
图3 全球COVID-19疫苗研发进展
最早投入使用的重组蛋白疫苗是俄罗斯Vector Institute研制的EpiVacCorona,原理是将化学合成的3条病毒刺突蛋白短肽链偶联到载体蛋白上,并加入铝佐剂(氢氧化铝)制成疫苗。该载体蛋白是重组表达的新冠病毒核衣壳蛋白和大肠杆菌麦芽糖结合蛋白(MBP)的嵌合体。2020年10月,该疫苗启动了三期临床试验,并于同期获得俄罗斯政府批准用于大规模国民接种运动。因为项目的早期实验数据被质疑存在缺陷,该疫苗是否足够安全有效尚无明确结论。
除此之外,在2020年底进入三期实验的Novavax 三聚体S重组蛋白疫苗目前得到了更为普遍的认可。2021年3月,Novavax宣布疫苗针对原始冠状病毒的有效率为96%,针对B.1.1.7突变株的有效率为86%,针对B.1.351突变株的有效率为49%。其制备方法是将改造过的三聚体S全长蛋白用纳米颗粒包裹,加入Novavax自家**的Matrix-M佐剂制成一剂疫苗。其中,S蛋白的两个关键改造,一是使用了S-2P技术,插入了两个可以稳定蛋白结构的脯氨酸(K986P和V987P),二是在Furin酶切位点加入了三个突变(R682Q、R683Q和R685Q),以避免刺突蛋白的S1和S2亚基解离形成免疫原性较低的与受体融合后构象。Matrix-M佐剂通过增强注射部位和淋巴结中的抗原呈递,可以进一步增强免疫应答,刺激人体产生高水平中和抗体。这些重组蛋白的纳米颗粒保留了天然病毒的空间构象,但它们无法复制和引起感染,因此安全性很高。并且,与Pfizer-BioNTech和Moderna的RNA疫苗相比,Novavax的疫苗可以在冰箱中保持稳定长达三个月的时间,更易于分发和存储。
其它正在进行1/2期临床试验的重组蛋白疫苗包括赛诺菲(Sanofi)和葛兰素史克(GSK)合作开发的COVID-19佐剂疫苗,三叶草生物制药(Clover)的SCB-2019疫苗,古巴基因工程与生物技术中心(CIGB)的CIGB-66疫苗,古巴Finlay研究所的FINLAY-FR-1、FINLAY-FR-2疫苗,以及受到2019冠状病毒病疫苗实施计划(COVAXX)支持、由联合生物医学公司(UBI)主导开发的UB-612疫苗等。
重组蛋白疫苗可能是迄今为止最兼具免疫原性和安全性的疫苗,但它们在第一批候选名单中并未被包括在内,可能是因为创新性较强的RNA疫苗和安全性较高的灭活病毒疫苗在疫情早期吸引了更多关注和资金。然而,随着多个重组蛋白疫苗在研究和试验中展现出不凡的效力和独特的优势,重组蛋白疫苗有潜力成为遏制新冠疫情的长期对策。
新冠重组蛋白疫苗的开发,需先经过临床前动物实验确定疫苗的免疫原性和安全性。如果疫苗能够引发动物产生免疫反应,随后将分三期临床试验在人体中进行测试,并且接种群体规模逐步扩大。在临床前和临床试验中,都需要对疫苗的免疫原性(IgG抗体滴度)和有效性(中和抗体滴度)进行检测,此外还会对疫苗可能产生的ADE效应(IgG抗体亚型滴度)进行评估。在得出所有这些临床试验的结果后,各国公共卫生部门对疫苗的有效性和安全性进行严格审查,才会将疫苗纳入国家免疫规划中并实行监管。
在临床试验结束进行疫苗大规模生产过程中,为监管疫苗的抗原含量,需要用配对抗体或抗原检测试剂盒来做抗原定量;为评估疫苗的抗原活性,需要用受体蛋白ACE2或抗体检测与疫苗样本的结合活性,以保证抗原的性质达到标准。
为助力加速疫苗研发,ACROBiosystems基于在重组蛋白领域多年的深耕和技术积累,针对新冠重组蛋白疫苗研究领域开发了多种试剂盒、抗原、抗体等核心试剂,可用于重组蛋白疫苗的研发生产质控和疫苗有效性评价。
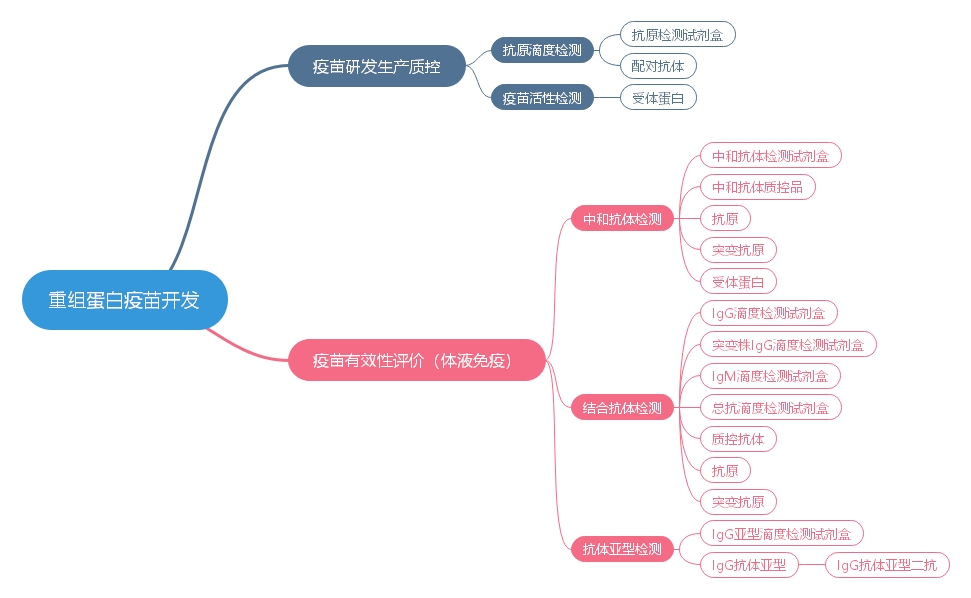
图4 ACROBiosystems可提供应用于重组蛋白疫苗开发各阶段的产品
| 应用领域 | 类别 | 相关产品 |
| 疫苗研发生产质控 | 抗原滴度检测 | 抗原检测试剂盒 |
| 配对抗体 | ||
| 疫苗活性检测 | 受体蛋白 | |
| 疫苗有效性评价 (体液免疫) |
中和抗体检测 | 中和抗体检测试剂盒 |
| 中和抗体质控品 | ||
| 抗原 | ||
| 突变抗原 | ||
| 受体蛋白 | ||
| 结合抗体检测 | IgG滴度检测试剂盒 | |
| 突变株IgG滴度检测试剂盒 | ||
| IgM滴度检测试剂盒 | ||
| 总抗滴度检测试剂盒 | ||
| 质控抗体 | ||
| 抗原 | ||
| 突变抗原 | ||
| 抗体亚型检测 | IgG亚型滴度检测试剂盒 | |
| IgG抗体亚型 | ||
| IgG抗体亚型二抗 |
订购、询价请扫描文末二维码添加小助手咨询
IgG滴度检测试剂盒(RBD) (货号:RAS-A021)
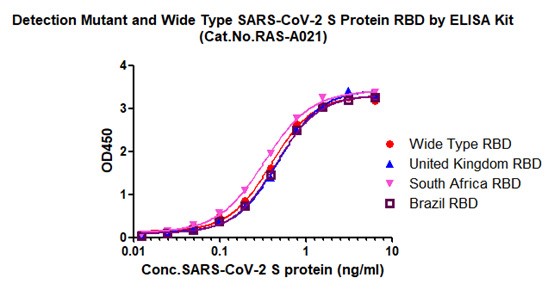
图5 抗原检测试剂盒可检测不同突变蛋白含量
订购、询价请扫描文末二维码添加小助手咨询
中和抗体滴度检测试剂盒(货号:TAS-K022)
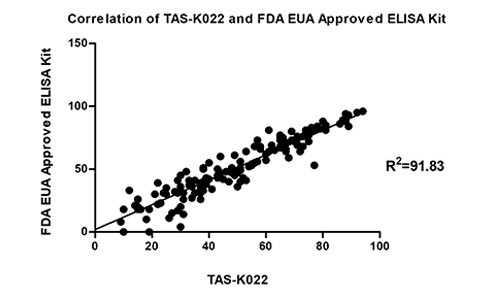
图6 中和抗体试剂盒与FDA EUA批准同类产品相关性好(检测接种疫苗后血清中中和抗体滴度)
订购、询价请扫描文末二维码添加小助手咨询
抗体亚型检测试剂盒(货号: RAS-T014/ RAS-T015/ RAS-T016/ RAS-T017)
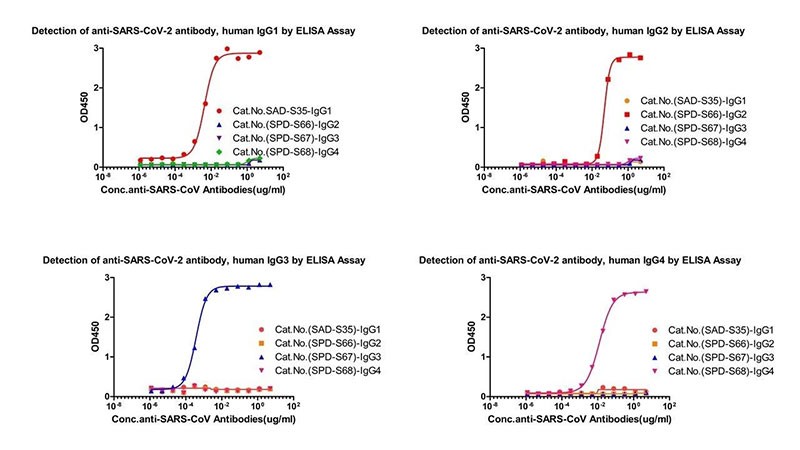
图7 抗体亚型检测交叉验证数据图
订购、询价请扫描文末二维码添加小助手咨询
广谱型中和抗体(货号:S1N-M122)
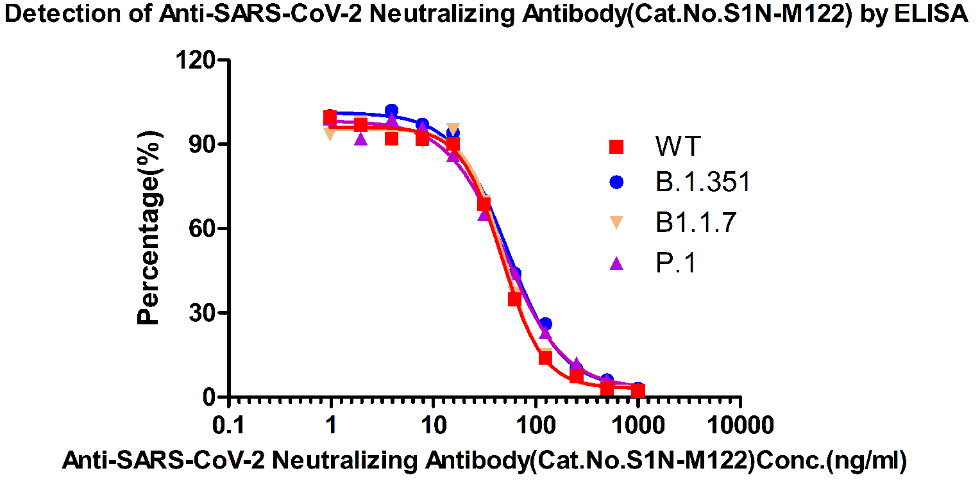
图8 ELISA方法检测中和抗体S1N-M122对突变株的中和能力
订购、询价请扫描文末二维码添加小助手咨询
您可通过以下方式联系到ACROBiosystems:
邮件:inquiry@acrobiosystems.com
电话:15117918562
微信:扫描下方二维码即可进行沟通

(请备注公司+姓名)
参考资料 :
1. An Y., Li S., Jin X, et al. A tandem-repeat dimeric RBD protein-based COVID-19 vaccine ZF2001 protects mice and nonhuman primates. bioRxiv 2021.03.11.434928; Retrieved from https://doi.org/10.1101/2021.03.11.434928
3. Dong Y., Dai T., Wei Y., et al. A systematic review of SARS-CoV-2 vaccine candidates. Signal Transduct Target Ther. 2020; 5: 237. Retrieved from https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7551521/
4. Krammer, F. SARS-CoV-2 vaccines in development. Nature 586, 516–527 (2020). Retrieved from https://doi.org/10.1038/s41586-020-2798-3
5. Pollet J, Chen WH, Strych U. Recombinant protein vaccines, a proven approach against coronavirus pandemics. Adv Drug Deliv Rev. 2021 Mar; 170:71-82. doi: 10.1016/j.addr.2021.01.001. Retrieved from https://pubmed.ncbi.nlm.nih.gov/33421475/
6. Tian, JH., Patel, N., Haupt, R. et al. SARS-CoV-2 spike glycoprotein vaccine candidate NVX-CoV2373 immunogenicity in baboons and protection in mice. Nat Commun 12, 372 (2021). Retrieved fromhttps://doi.org/10.1038/s41467-020-20653-8
7.Wikipedia contributors. EpiVacCorona. In Wikipedia, The Free Encyclopedia. 2021. Retrieved from https://en.wikipedia.org/w/index.php?title=EpiVacCorona&oldid=101981146 8
8. Yadav T, Srivastava N, Mishra G, Dhama K, Kumar S, Puri B, Saxena SK. Recombinant vaccines for COVID-19. Hum Vaccin Immunother. 2020 Dec 1;16(12):2905-2912. Retrieved from https://pubmed.ncbi.nlm.nih.gov/33232211/

